- 首頁
- 我們的服務
-
項目簡介
醫療器械檢測是確保產品安全、有效與合規的關鍵環節,涵蓋性能驗證、材料安全及生物相容性測試,旨在預防潛在風險,保護患者健康,推動行業持續發展。
服務項目
醫用敷料類、醫用輸注器具及醫用導管類、藥械組合醫療器械、醫美產品
服務優勢
資質完備:已獲得國家CMA、省級CMA及CNAS資質,檢測結果權威可靠。
項目全面:提供理化/微生物檢測、生物相容性研究(依據GB/T 16886/ISO 10993)及臨床前功能性評價的一站式服務。
專業團隊:擁有經驗豐富的檢測隊伍,精通各類醫療器械標準與流程,確保高效精準服務。
風險控制:通過體外/體內實驗綜合評價產品安全性,助力產品合規上市,提升市場競爭力。
-
服務簡介
華微檢測是由廣州高新區投資集團直屬單位聯合華南新藥創制中心及海歸技術團隊共同建設的第三方檢測機構,專注生物安全、生物醫藥與動物實驗等領域。我們搭建生物制品分析檢測綜合平臺,嚴格遵循ISO/IEC17025體系,已獲國家CMA和CNAS認證,提供符合《中國藥典》要求的細胞系/株全面檢定服務,適用于抗體、重組蛋白、疫苗、細胞基因治療產品等生物制品的合規報批。
服務項目
細胞庫檢測、生物制品批放行檢查/型式檢查、細胞內外源病毒因子檢查、原輔料/培養基/耗材檢查、工藝雜質殘留研究、微生態制劑(活菌制劑)檢查
服務優勢
權威資質:通過CMA、CNAS認證,實驗室符合GMP體系,檢測結果具法律效力和國際公信力。
高標準實驗室:配備多間加強型P2實驗室(廣州市備案),B+A環境,滿足無菌及病毒檢測要求。
法規符合性強:嚴格遵循FDA、CHP、EP、ICH等國際國內法規,建立全面細胞庫檢定流程。
專業團隊與技術:依托高水平技術團隊和完備操作規程,為客戶提供精準、高效的生物制品檢測服務。
-
服務簡介
我司提供全面的藥代藥效學研究評價服務。我們嚴格遵循NMPA、FDA和ICH相關技術指導原則,為客戶提供符合申報要求的全套體內外評價模型與試驗數據支持。
服務項目
藥代動力學研究、 藥效學研究、皮膚外用試劑透皮吸收研究
服務優勢
綜合平臺:整合藥代、藥效及透皮研究能力,提供從體外到體內的一體化評價方案。
專業團隊:擁有經驗豐富的研究人員,精通各類藥物劑型與模型的評價標準與法規要求。
先進設備:配備LC-MS/MS、高效滲透系統等先進儀器,保證數據精準、可靠。
合規高效:實驗過程嚴格遵循GLP規范,支持國內外注冊申報,加速產品研發與上市進程。
-
服務簡介
華微檢測提供專業的藥品及原輔料質量研究與檢測分析服務,配備精密儀器實驗室、核磁共振實驗室及多類先進分析設備,涵蓋理化性質分析、雜質研究、含量測定及方法開發與驗證等項目,全面支持藥品研發、生產及注冊申報的質量控制需求。
服務項目
藥品/原輔料理化檢查、藥品微生物檢查、效價與生物學活性、生物安全性檢測(生物制品)、抗菌/抗病毒藥物篩選
服務優勢
設備先進齊全:配置HPLC、LC-MS、GC-MS、ICP-MS、AAS、酶標儀等多類型高端儀器,保證檢測數據精準可靠。
技術能力深厚:具備藥品及原輔料方法開發與驗證經驗,可提供從常規檢測到復雜研究的全流程解決方案。
定制化服務:依據企業實際需求,提供靈活、高效的定制化開發與檢測服務,助力企業加速研發進程。
平臺資源豐富:依托完備的實驗室平臺和專業團隊,能夠同時應對多品類、多標準的藥品質量評價任務
-
服務簡介
新型冠狀病毒疫情嚴重危害人類健康,已成為全球關注的公共衛生問題。抗病毒材料作為一種重要的防護手段,可有效抑制和殺滅病毒,但其實際效果需通過專業檢測驗證。 隨著疫情防控常態化,市場對消毒及健康防護產品的需求持續增長,相關企業對于產品檢測的需求也日益迫切。 華微檢測為企業提供抗病毒材料及病毒消殺產品的專業檢測服務,助力產品有效性驗證,為公共健康保駕護航。
服務項目
凈化產品病毒去除性能測試、消毒產品病毒滅活效果測試、日化輕工材料抗病毒效果測試、精品定制化服務
服務優勢
精英團隊,背景多元:技術團隊由廣微所、華南新藥創制中心、高校重點實驗室人員及病毒學領域海歸博士專家組成,結構合理、實戰經驗豐富。
頂尖設備,科研級服務:依托先進硬件設施與高層次科研隊伍,在常規檢測中提供深度、沉浸式的科研體驗。
靈活定制,一站式支持:除標準化測試外,支持各類客供實驗方案,為產品開發與課題研究提供精品化、全方位技術服務。
-
服務簡介
食品保健品檢測是通過理化、微生物與毒理學等方法,對食品及保健品的成分、安全性、功效及標簽合規性進行全面分析的科學過程。 我們致力于通過檢測重金屬、農殘、微生物等風險物質,保證產品安全;驗證有效成分與宣稱功能,確保功效可信
服務項目
食品保健品毒理學檢測、食品保健品功效評價研究、其它定制化服務
服務優勢
符合國家標準與國際法規,助力市場準入; 具第三方檢測報告,增強消費者信任,提升產品競爭力。
-
華微檢測除核心檢測服務外,還可提供以下延伸技術支持:專業實驗空間租賃、定制化實驗方案設計、規范化的實驗動物代養 實驗方案設計是決定科研成敗與數據可靠性的關鍵環節。我們憑借專業團隊和豐富經驗,協助客戶根據研究目標與條件,設計科學、嚴謹、可操作的實驗方案,為項目順利開展提供堅實基礎。
- 新聞資訊
- 檢測流程
- 下載中心
- 關于我們
- 聯系我們
 新聞資訊INFORMATION CENTER標準解讀丨MSCs國際新規發布,定義統一促臨床應用規范化!
新聞資訊INFORMATION CENTER標準解讀丨MSCs國際新規發布,定義統一促臨床應用規范化! 2741次
2741次 2025-07-30
2025-07-30
標準解讀丨MSCs國際新規發布,定義統一促臨床應用規范化!
國際細胞與基因治療協會(International Society for Cell and Gene Therapy,ISCT)于2024年10月28日發布了新版間充質基質細胞(Mesenchymal Stromal Cells, MSCs)的鑒定標準,并將這一鑒定標準發布在旗下雜志Cytotherapy上。相比一直沿用至今的2006年舊版標準,此次修訂作出重要調整:首先,明確定義術語使用規范,將“MSCs”統一命名為“間充質基質細胞”,若采用“間充質干細胞”命名則需提供證明其干性的驗證數據,同時傳統干性判定指標(包括體外三系分化能力及標準貼壁生長特性)也被排除在鑒定建議之外;其次,新標準強化了各方面的質量控制體系,如細化了細胞標志物要求并需設定流式檢測閾值與結果百分比、嚴格規定組織來源標識、加強對效力與特性的關鍵質量屬性評估等。
此次標準更新,將終結行業長久以來對MSCs身份的爭論,標志著MSCs臨床應用正式進入以明確生物學特性為基礎的精準治療階段。

自MSCs于1995年首次作為治療劑開展試驗以來,其在不同疾病臨床前模型中顯示出療效,展示了巨大的潛力,但其針對各類適應癥的臨床試驗結果卻未能達到預期。多項因素可解釋MSCs療法臨床轉化面臨的挑戰,其中較關鍵的是:臨床前與臨床研究中使用的MSCs在關鍵特性(如細胞表征、免疫相容性、存活率及給藥劑量)上存在顯著差異。為提高MSCs研究領域的臨床轉化性、可重復性與透明度,科學界需就MSCs的定義達成共識,本次多家相關機構通過正式的共識流程——即德爾菲法——制定基于共識的MSCs定義及MSCs療法臨床試驗報告指南。
關于MSCs定義與表征
較低標準共識的新舊版本對比
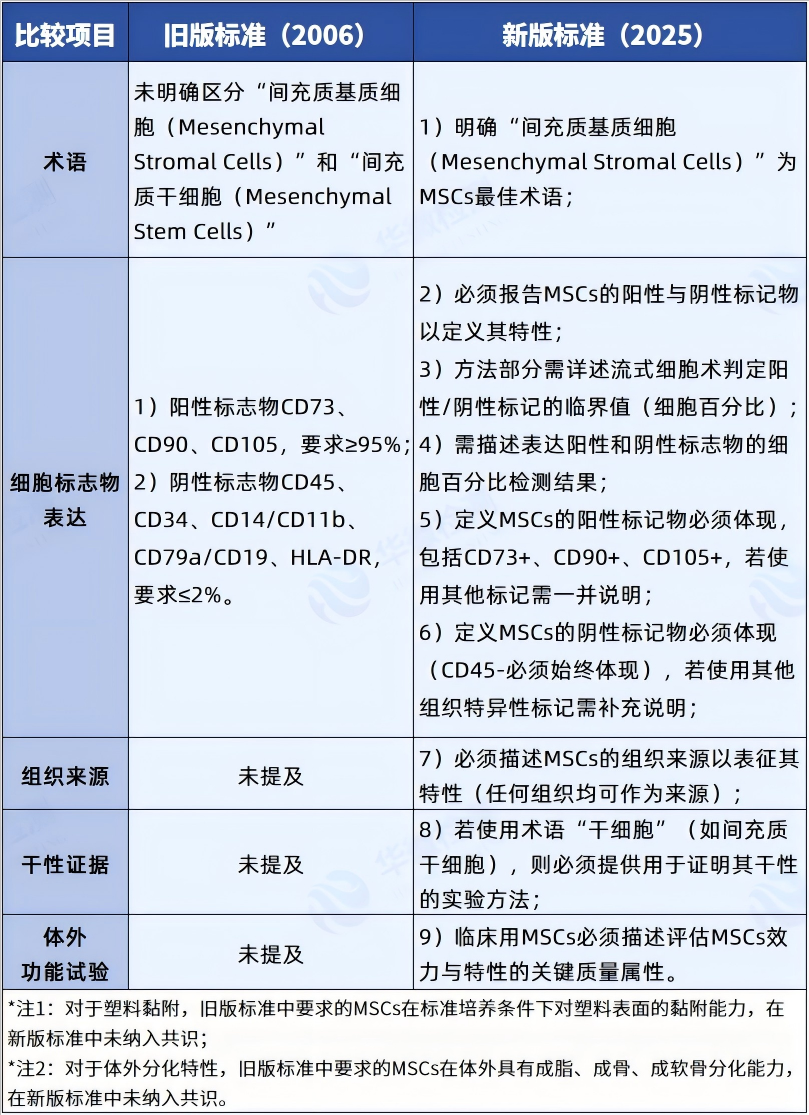
新版標準除給出上述9項MSCs定義與表征的共識標準內容之外,關于MSCs臨床研究報告指南共識另有33項條目納入了共識,包括MSCs干預組與對照組(9項)、MSCs特性14項、MSCs培養條件(10項),有興趣的朋友記得關注我們下期內容。
“間充質干細胞(Mesenchymal Stem Cells)”與“間充質基質細胞(Mesenchymal Stromal Cells)”雖共享“MSCs”縮寫,但卻是兩類截然不同的細胞群體。2006年ISCT首次提出MSCs鑒定標準并作為MSCs行業共識一直沿用至今,但該版標準未能有效區分這兩類細胞,導致臨床實踐中仍將MSCs視為干細胞開展應用。這種對MSCs身份的認知錯位直接導致了MSCs臨床效果的不穩定,嚴重阻礙了行業發展。
此次,ISCT基于德爾菲共識法(Delphi方法)將全球專家的研究意見進行科學匯總,并分3輪次對其中的每一項鑒別指標進行投票,較終得出了代表了全球頂尖專家對MSCs的共識標準,但研究分析仍然不可避免存在以下局限:
1. 參與者多樣性不足
1)首輪參與率低;
2)地域代表性失衡:北美地區代表過多,亞洲、非洲代表不足。
2. 定義范疇的局限性
1)臨床實體導向:當前共識將MSCs定義為臨床實體(而非特定細胞類型或混合群體);
2)標記物陽性細胞頻率(如CD73+細胞的較低比例);
3)功能檢測標準化(如干性驗證的具體實驗方法);
4)生物學機制整合不足:對MSC體內作用機制的新認知(如免疫調節途徑)尚未充分融入定義框架。
MSCs名稱的更迭絕非簡單的術語之爭,而是國際科學共同體對其生物學本質的較終確認。這一科學范式轉型將重構從基礎研究到臨床轉化的全鏈條認知體系——當“間充質基質細胞療法”取代既往模糊的“干細胞治療”概念,實則是為細胞治療產品建立了可驗證的質量基準與風險控制框架。新標準推動的不僅是命名規范,更是全球學界、監管機構與產業界的協同進化:學術界亟待突破基質細胞作用機制研究,藥監部門需要建立適配的審評路徑,而產業界則面臨生產工藝與質控體系的重構。唯有完成這場細胞治療全生態的范式革命,才能真正釋放間充質基質細胞的臨床價值,讓科學承諾轉化為切實的民生福祉。這場關乎生命科學產業格局變革的科學實踐,其歷史進程值得期待。
關于華微
廣東省華微檢測股份有限公司(簡稱“華微檢測”)由廣州高新區集團主導,廣州市微生物研究所與華南新藥創制中心共同組建。現為國家高新技術企業、廣東省專精特新企業、瞪羚培育企業、廣東省科技中小型企業、廣東省創新性中小企業,廣州開發區、黃埔區生物制品行業質量基礎設施服務工作站。致力于為醫療器械、生物安全、生物制品等生物醫藥領域企業和和研發機構提供全流程、一站式質量檢測分析及科學研究服務。
華微檢測在政府相關部門指導下建設了廣州市首家生物制品分析檢測綜合服務平臺,包括細胞質量研究與技術服務平臺、廣東省生物種質資源庫病毒庫、廣東省藥代動力學重點實驗室、GMP質量體系運行管理平臺等,實驗室嚴格遵照ISO/IEC17025標準規范要求運行,并已取得國家CMA與CNAS等第三方檢測機構相關資質證書。
平臺定位:華微檢測-廣東華南新藥創制中心聯合檢測實驗室
生物制品標準品研發
非法定業務檢測:細胞治療(MSC、CAR-T、IPSC細胞等)、疫苗、抗體及分子診斷
生物制品檢測標準方法研究


- 服務范圍
生物制品服務工作站 +
廣州開發區廣州市黃埔區生物制品行業質量基礎設施服務工作站
特色檢測服務 +
微生物制劑評價
抗菌抗病毒藥物篩選
抗生素效價檢測
醫療器械檢測 +
醫用敷料檢測
醫用輸注器具及醫用導管檢測
藥械組合醫療器械檢測
醫美產品檢測
生物制品檢測 +
細胞庫檢測
生物制品批放行檢查/型式檢查
細胞內外源病毒因子檢查
原輔料、培養基、耗材檢查
工藝雜質殘留研究
微生態制劑(活菌制劑)檢查
非臨床研究與生物樣本檢測 +
藥代動力學研究
藥效學研究
皮膚外用制劑透皮吸收研究
樣本分析檢測
病毒中和抗體檢測
藥品檢測 +
藥品、原輔料理化檢查
藥品微生物檢查
效價與生物學活性
抗菌/抗病毒藥物篩選
藥包材檢測
病毒殺滅檢測 +
凈化產品病毒去除性能測試
消毒產品病毒滅活效果測試
日化輕工材料抗病毒效果測試
精品定制化測試
食品/保健食品檢測 +
食品保健品毒理學檢測
食品保健品功效評價研究
其它定制化服務
其他檢測服務 +
化妝品原料毒理檢測
化妝品體外功效評價
化妝品/美容儀體內外透皮吸收評價
實驗動物飼/寄養服務
動物誘發性造模
儀器設備共享服務
分子生物學實驗技術服務平臺
ELISA實驗技術服務
熒光定量PCR實驗技術服務
Western Blotting實驗技術服務
外源性生物殘留檢測服務平臺
病毒核酸參考品服務
- 聯系我們
- 聯系人:史工18928790749、嚴工
- 手機:19924323595、020-82118202、020-31608627【微信同號】
- 微信號:
掃碼添加史工 掃碼添加嚴工
- 郵箱:yanyongxian@gdhvt.com
- 地址:廣州市黃埔區攬月路3號F棟316(總部)廣州市黃埔區科學城尖塔山路1號(動物中心)

 為您推薦更多
為您推薦更多

掃碼添加史工 掃碼添加嚴工
聯系人:史工18928790749、嚴工
聯系電話:19924323595、020-82118202、020-31608627
地址:廣州市黃埔區攬月路3號F棟316(總部)廣州市黃埔區科學城尖塔山路1號(動物中心)
版權所有 ? 廣東省華微檢測股份有限公司- 生物制品服務工作站
- 特色檢測服務
- 醫療器械檢測
- 生物制品檢測
- 非臨床研究與生物樣本檢測
- 藥品檢測
- 病毒殺滅檢測
- 食品/保健食品檢測
- 其他檢測服務
-




 立即咨詢
立即咨詢 留言咨詢
留言咨詢



